La norma ISO 16140:2003, para la validación de métodos microbiológicos en la cadena alimentaria, se ha utilizado con éxito durante años, dando por resultado más de 100 métodos alternativos validados, que son de uso general por laboratorios en pruebas de rutina. Desde el junio pasado, la norma ha sido actualizada y reestructurada por la ISO, con cambios relevantes respecto a la anterior versión.
La ISO 16140, una herramienta para la seguridad alimentaria
La versión revisada de la norma ISO 16140 fué publicada el pasado mes de junio como ISO 16140-2:2016 Protocolo para la validación de métodos alternativos (registrados) frente a los métodos de referencia. Se trata de la segunda parte de la norma, de un total de 6.
Esta norma, aceptada a nivel europeo e internacional, es de aplicación en el campo de la microbiología de la cadena alimentaria, incluyendo toda la cadena de producción de alimentos; desde la producción primaria, los entornos de procesamiento, manipulación y almacenamiento de alimentos, hasta el producto final.
La comprobación de la presencia o el nivel de microorganismos patógenos e indicadores de higiene (bacterias, levaduras y mohos, virus y parásitos) es crucial para garantizar la inocuidad de los alimentos, por lo que la ISO 16140 es una herramienta que facilita la seguridad alimentaria, al permitir validar métodos microbiológicos más rápidos o económicos que los de referencia pero igualmente eficaces para determinados propósitos.
Hace pocos dias informábamos de la publicación en castellano de la nueva versión de la norma, publicada en la web de AENOR. Hoy recogemos los comentarios de miembros del comité ISO/TC 34/SC 9, responsable de la revisión de la norma, acerca de los cambios que ésta ha introducido en la anterior versión, publicados en un artículo de la revista Food Quality and Safety.
Según los autores del artículo, el principio para las dos versiones sigue siendo el mismo: un protocolo que describe la validación de métodos cualitativos y métodos cuantitativos, que requieren diferentes parámetros de rendimiento.
En ambos casos, la validación se basa en: un estudio de comparación de métodos, realizado en un laboratorio especialista y un estudio inter-laboratorio, dirigido por el mismo laboratorio especialista. Se seleccionan parámetros de rendimiento, cada uno con una definición, un diseño experimental, cálculos e interpretación de resultados.
Con la revisión de la norma, los detalles para la realización de los estudios y la interpretación de los resultados se han modificado sustancialmente en ciertos aspectos:
Los cambios principales en la validación de métodos cualitativos
Concepto de estudio emparejado y no emparejado
El primer cambio importante es la introducción del concepto de estudio "emparejado" y "no emparejado". Un estudio emparejado es aquel en que el método de referencia y los métodos alternativos utilizan el mismo primer paso en el protocolo de enriquecimiento. Por ejemplo el pre-enriquecimiento de Salmonella en agua de peptona tamponada durante 16 -20 horas a 37 ºC.
En el caso de un estudio no emparejado, el primer paso en el método de referencia y en los alternativos no es idéntico. Por ejemplo el uso de un caldo de enriquecimiento específico distinto del agua de peptona tamponada en los métodos alternativos. En este caso se deben ensayar porciones de prueba separadas (de la misma muestra), para el método de referencia y para los alternativos. Esto parece un cambio técnico pero tiene un impacto importante en la interpretación de los resultados.
En un estudio emparejado, es fácil determinar cuando un resultado es falso-negativo (positivo por el método de referencia pero negativo por el método alternativo). Cuando el método de referencia da un resultado positivo, el método alternativo también debe tener un resultado positivo, ya que se ha comprobado que la muestra contiene el microorganismo diana.
Pero en un estudio no emparejado ya no existe un vínculo directo entre el resultado obtenido con el método de referencia y los alternativos, ya que se utilizan diferentes porciones de prueba. Esto es determinante especialmente cuando el nivel de contaminación de las muestras es muy bajo. Para los métodos cualitativos, el nivel de contaminación debe ser muy bajo para demostrar que los métodos alternativos son eficaces, pero la heterogeneidad causada por los bajos niveles de contaminación conduce a diferencias entre las porciones de prueba, dado que algunas de ellas ya no contendrán el organismo diana y, por tanto, no daran positivo.
Limites de Aceptabilidad
Para la interpretación de los resultados también se introduce un concepto nuevo. La evaluación de los resultados se basa en los llamados Limites de Aceptabilidad, basados en la evaluación de estudios previos de validación y en la opinión de expertos. Los Limites de Aceptabilidad se basan en el número de desviaciones positivas y negativas observadas en el estudio de validación, y se determinan los valores máximos aceptables para los estudios emparejados y no emparejados.
Nivel Relativo de Detección
Otra diferencia importante respecto a la ISO 16140:2003 es la introducción del concepto Nivel Relativo de Detección, en el que los dos métodos se comparan utilizando las mismas muestras, contaminadas artificialmente. El nivel de contaminación debe ser muy bajo, para que no todas las muestras probadas sean positivas para el organismo diana. Mediante la prueba de muchas réplicas en este nivel bajo, se pueden observar las diferencias en el número de positivos encontrados por el método de referencia y los alternativos. La diferencia observada se compara entonces con un Limite de Aceptabilidad preestablecido.
Los cambios principales en la validación de métodos cuantitativos
Estudio de veracidad relativa
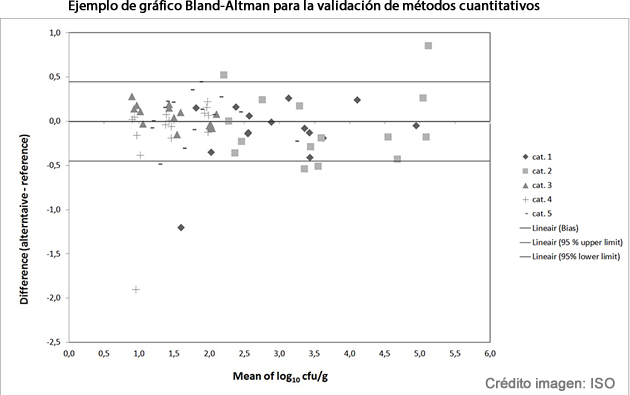
El estudio de "linealidad y precisión" se reemplaza por un estudio de "veracidad relativa". El diseño experimental de esta parte del estudio de validación no cambia respecto a la ISO 16140: 2003 pero la evaluación de los datos si. La regresión lineal ya no se lleva a cabo y los datos se representan de dos maneras diferentes; como un gráfico de dispersión y como un gráfico de Bland-Altman.
El diagrama de dispersión da una impresión de la linealidad de los resultados y en el gráfico de Bland-Altman se representa la diferencia entre el resultado del método alternativo (log10 transformado) y el resultado del método de referencia (log10 transformado) para cada muestra individual. Este gráfico contiene también datos de las muestras en las que uno de los dos métodos ha dado un resultado fuera del limite de cuantificación del método (por ejemplo, recuentos inferiores a 10 en una placa). Sobre la base de estos dos gráficos, se interpretan los datos y aquellos resultados que aparezcan visualmente aislados o periféricos deben ser investigados para explicar la causa de esta variación.
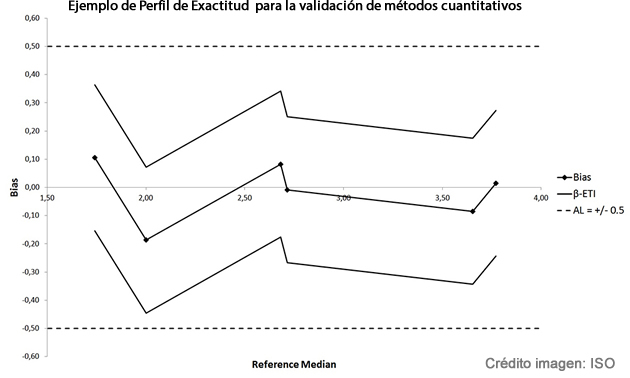
Estudio de perfil de exactitud
Otro cambio importante es la introducción del estudio de "perfil de exactitud", una combinación de pruebas de sesgo y precisión. Los cálculos se basan en un intervalo de tolerancia y la evaluación de los datos se realiza utilizando un Limite de Aceptabilidad de 0,5 log en el caso general. Los resultados se representan como en el gráfico a continuación.
Próximas partes en desarrollo de la ISO 16140
Como ya comentabamos en un artículo anterior, la nueva versión de la norma ISO 16140 está estructurada en seis partes, de las cuales la primera ISO 16140-1:2016 Vocabulario ya está publicada.
Actualmente, los expertos que han desarrollado la segunda parte de la norma, está trabajando en las cuatro partes siguientes.
La parte 3 Protocolo para la verificación de métodos de referencia y métodos alternativos validados aplicados en un laboratorio único , tendrá especialmente un fuerte impacto en todos los laboratorios que realicen análisis en la microbiología de la cadena alimentaria. La verificación del método es el estudio que el laboratorio debe realizar para demostrar su competencia en la aplicación de un método validado en su propio laboratorio.
Las partes 4 Protocolo para la validación del método en un laboratorio único (interno) y 5 Protocolo para la validación factorial entre laboratorios de métodos no registrados, ofrecerán nuevas oportunidades para los laboratorios que operan en pruebas de microbiología alimentaria.
La sexta y última parte Protocolo para la validación de métodos alternativos (registrados) para la confirmación y el tipificado microbiologico, proporcionará un protocolo técnico para la validación de métodos patentados para la confirmación de aislamientos, lo que es también un concepto nuevo.
El desarrollo de estas cuatro normas sigue su curso y se espera que las versiones para consulta pública estén disponibles en 2017. El proceso de aprobación formal se iniciará probablemente en 2018.
Fuentes: Food Quality and Safety, ISO








